TIPOS DE CADENA E ISOMERÍA
Las propiedades de las diversas sustancias y los usos de un material dependen de su estructura molecular.
Métodos para conocer la estructura de las moléculas.
1.-Se considera la fuerza de repulsión entre los pares de electrones que estás alrededor de un átomo.
2.- Toma en cuenta las distintas maneras de los orbitales atómicos pueden combinarse para formar orbitales alrededor de más de un núcleo.
3.- Las moléculas tienen más de una estructura posible.
4.- Considera a los orbitales de las moléculas como una unidad y no como orbitales pertenecientes a átomos individuales.
Tipos de cadenas.
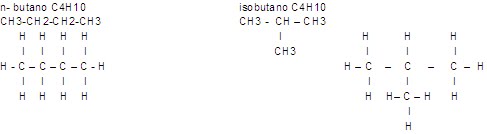
Debido a su tetravalencia el átomo de carbono forma moléculas gigantes como el diamante o el grafito al combinarse de manera diferente. Se combina con otros átomos de carbono y forma lo que se llama longitud de enlace. El butano tiene una longitud de 4 ya que está formado por cuatro átomos de carbono enlazados entre sí.
La longitud de la cadena del carbono determina la mayoría de sus propiedades físicas, tales como si el punto de ebullición y la solubilidad. Los gases y líquidos que tienen bajo punto de ebullición son compuestos con cadenas cortas, los compuestos con cadenas medianas son líquidos mientras que los sólidos tienen cadenas largas.
TIPOS DE FORMULA UTILIZADOS EN QUÍMICA ORGÁNICA E ISOMERÍA.
Con la tetravalencia del átomo de carbono, los compuestos orgánicos se pueden representar mediante 3 tipos de fórmulas:
1.- Condensado o molecular.
2.- Semidesarrollada o de estructurada.
3.- Desarrollada o gráfica.
Fórmula condensada o molecular.- Indica sólo el número total de átomos de cada elemento del compuesto, por ejemplo: C4 H10.
FÓRMULAS DE LA QUÍMICA ORGÁNICA.
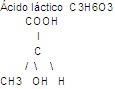
ISOMERÍA.- Tiene la misma fórmula condensada, pero diferente fórmula estructural o semidesarrollada. Son compuestos de igual fórmula molecular, pero con distintas propiedades.
1.- De cadena o estructural.
2.- De composición o lugar.
3.- Geométrica
4.- Óptica
5.- Funcional.
ISOMERÍA DE CADENA
ISOMERIA DE POSICIÓN
ISOMERÍA GEOMETRICA
ISOMERÍA ÓPTICA
PROPIEDADES FÍSICAS, LA NOMENCLATURA Y EL USO DE LOS COMPUESTOS DEL CARBONO.
Hidrocarburos.- Son los compuestos más importantes obtenidos por el hombre, ya que de ellos se consigue una enorme variedad de productos petroquímicos. Antes eran sustancias puras, derivadas del petróleo y se empleaban sólo en la industria química. Como las compañías petroleras entraron al mercado químico las sustancias químicas se pueden considerar sustancias petroquímicas.
NOMENCLATURA DE HIDROCARBUROS ALIFÁTICOS.
Se clasifican según el número de enlaces covalentes formados entre los átomos de carbono de los compuestos. Se dividen en alifáticos y aromáticos.
Hidrocarburos alifáticos.- No contienen el grupo benceno o el anillo bencénico. Se divide en alcanos, cicloalcanos, alquenos y alquinos.
Hidrocarburos aromáticos.- Contienen uno o más anillos bencénico.
Alquenos.- Compuestos por doble enlace de carbono-carbono.
Alquinos.- Compuestos por triple enlace de carbono- carbono.
Alcanos.- Si hay enlaces carbono-carbono, son hidrocarburos saturados.
Radicales alquilo (R).- Es un átomo o grupo de átomos que constituye sólo parte de una molécula; en la estructura de un hidrocarburo saturado que ha perdido un átomo de hidrógeno, de manera que su nombre se deriva del hidrocarburo principal sustituyendo la terminación ano, il, ilo.